Тиамин биохимия. Биохимия ферментов
Витамин В 1 был первым витамином, выделенным в кристаллическом виде К. Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название – тиамин – этот витамин получил из-за наличия в составе его молекулы атома серы и аминогруппы.
Тиамин состоит из двух гетероциклических колец – аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу – карбанион (относительно кислый углерод между серой и азотом).
Тиамин хорошо сохраняется в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде, например при выпечке теста с добавлением соды или карбоната аммония, он быстро разрушается.
Метаболизм . В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть его всасывается в тонком кишечнике с помощью специфического механизма активного транспорта, остальное количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и ткани.
ТПФ-киназа
АТФ + Tиамин Тиаминпирофосфат + АМФ
Существует мнение, что основной транспортной формой тиамина является ТМФ.
Витамин В 1 присутствует в различных органах и тканях как в форме свободного тиамина, так и в форме его фосфорных эфиров: тиаминмонофосфата (ТМФ), тиаминдифосфата (ТДФ, синонимы: тиаминпирофосфат, ТПФ, кокарбоксилаз а) и тиаминтрифосфата (ТТФ).

ТТФ – синтезируется в митохондриях с помощью фермента ТПФ-АТФ-фосфотранс феразы:
Трансфереза
ТПФ + АТФ ТДФ + АМФ
Основной коферментной формой (60–80 % от общего внутриклеточного содержания) является ТПФ.
ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия. После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
Биохимические функции . Витамин В 1 в форме ТПФ является составной частью ферментов, катализирующих реакции прямого и окислительного декарбоксилирования кетокислот.
Участие ТПФ в реакциях декарбоксилирования кетокислот объясняется необходимостью усиления отрицательного заряда углеродного атома карбонила кетокислоты в переходном, нестабильном состоянии. Переходное состояние стабилизируется ТПФ путем делокализации отрицательного заряда карбаниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мультиферментных комплексов дегидрогеназ α-оксикетокислот (см. ниже).
1 . Участие ТПФ в реакции прямого декарбоксилирования пировиноградной кислоты (ПВК). При декарбоксилировании ПВК с помощью пируватдекарбоксилазы образуется ацетальдегид, который под воздействием алкогольдегидрогеназы превращается в этанол.ТПФ является незаменимым кофактором пируватдекарбоксилазы. Этим ферментом богаты дрожжи.

2 . Участие ТПФ в реакциях окислительного декарбоксилирования. Окислительное декарбоксилирование ПВК катализирует пируватдегидрогеназа . В состав пируватдегидрогеназного комплекса входят несколько структурно связанных ферментных белков и коферментов. ТПФ катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксилазой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки – цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей, заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплекса активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерола, стероидных гормонов, ацетоновых тел и др.
Окислительное декарбоксилирование α-кетоглутатарата катализирует α–кетоглута-ратдегидрогеназа. Этот фермент является составной частью цикла Кребса. Строение и механизм действия α-кетоглутаратдегидрогеназного комплекса схожи с пируватдегидрогеназой, т.е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла.
Помимо окислительных превращений ПВК и α-кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвленным углеродным скелетом (продукты дезаминирования валина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.
3. ТПФ – кофермент транскетолазы. Транскетолаза – фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается в том, что он является основным поставщиком НАДФH + H + и рибозо-5-фосфата. Транскетолаза переносит двууглеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату, что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и гептозы (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карбаниона, образующегося при расщеплении связи С2- С3 ксилулозо-5-фосфата.
4 . Витамин В 1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА – субстрата ацетилирования холина.
5. Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции, конкретный механизм которых еще нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врожденных тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В 1 как опосредованных стресс-реакцией.
Гиповитаминоз. Уже ранние проявления гиповитаминоза сопровождаются снижением аппетита и тошнотой. Отмечаются неврологические расстройства, к которым относятся нарушение периферической чувствительности, ощущение ползания «мурашек», невралгии. Характерна забывчивость, особенно на недавние события. Слабость сердечной мышцы проявляется тахикардией даже при незначительных нагрузках.
Недостаток в пище тиамина приводит к значительному накоплению пировиноградной и α-кетоглутаровой кислот, снижению активности тиаминзависимых ферментов в крови и тканях организма.
В эксперименте показано, что тиаминовая недостаточность сопровождается нарушением структуры и функции митохондрий. Добавление к последним ТПФ нормализует тканевое дыхание. У белых крыс, лишенных таимина, развивалась анорексия, уменьшалась масса тела. Шерсть теряла свой блеск, становилась взъерошенной. Животные мало двигались и обычно лежали, свернувшись в углу клетки. Анорексия является результатом резкого угнетения секреции желудочного сока и ослаблением его переваривающей способности.
Алиментарная недостаточность тиамина у человека приводит к патологическим изменениям в нервной, сердечно-сосудистой и пищеварительной системах, сопровождаясь общим истощением организма.
Болезнь бери-бери возникает при значительном дефиците тиамина и характеризуется крайне тяжелым течением. В прошлом веке в странах Востока она унесла миллионы жизней. Бери-бери в переводе с индийского означает «овца». Походка больного, действительно, похожа на поступь овцы (симптом симметричного опускания стоп). Поскольку у заболевших отмечалась тяжесть в ногах и скованность походки, бери-бери называлась также «кандальной болезнью». Этим заболеванием часто страдали заключенные, рацион питания которых состоял в основном из очищенного риса. Проявление недостаточности тиамина можно наблюдать до сих пор у бедных лиц в тех странах, где основу питания населения составляет полированный рис – в шлифованном зерне, в отличие от неочищенного, нет этого витамина. Последняя эпидемия бери-бери была на Филиппинах в 1953 г (погибло 100 000 человек).
Болезнь имеет две формы: сухую (нервно-паралитическую) и отечную (сердечную). Причем в обоих случаях поражаются и сердечно-сосудистая и нервная системы, но в разной степени. В настоящее время классической бери-бери, по-видимому, уже нет, однако явления умеренного гиповитаминоза отмечаются часто. К основным симптомам недостаточности тиамина относятся: физическая слабость, снижение аппетита (витамин В 1 необходим для стимуляции желудочной секреции), стойкие запоры; расстройство функции нервной системы (онемение пальцев, чувство «ползания мурашек», утрата периферических рефлексов, боль по ходу нервов); нарушения психической деятельности (раздражительность, забывчивость, страх, иногда галлюцинации, снижение интеллекта). Позже развивается глубокое поражение нервной системы, характеризующееся потерей чувствительности конечностей, развитием параличей, атрофией мышц в результате нарушения их иннервации. При отечной форме, наряду с явлениями полиневрита, отмечаются тахикардия и одышка даже при незначительных нагрузках. Из-за слабости сердечной мышцы развиваются отеки. Особенно часто проявления тиаминовой недостаточности наблюдаются у хронических алкоголиков вследствие их склонности больше пить, чем есть. Синдром Вернике, развивающийся у этих лиц, характеризуется нарушением координации движений, зрительной функции, спутанностью сознания.
Особая чувствительность нервной ткани к недостатку тиамина объясняется тем, что коферментная форма этого витамина абсолютно необходима нервным клеткам для усвоения глюкозы, которая является для них почти единственным источником энергии (большинство других клеток организма может использовать иные энергетические вещества, например жирные кислоты). Кстати, питание преимущественно углеводной пищей (белый хлеб, сладости) приводит к повышенной потребности в тиамине и, следовательно, к развитию вторичной тиаминовой недостаточности.
Существуют врожденные нарушения обмена тиамина, наиболее распространенным из которых является синдром Вернике-Корсакова. В основе этого синдрома, сопровождающегося потерей памяти и частичным параличом, лежит изменение свойств фермента транскетолазы, у которой уменьшается сродство к ТПФ. Гены других ТПФ-зависимых ферментов не затрагиваются. Заболевание проявляется, если уровень потребляемого ТПФ снижается ниже значений, необходимых для насыщения транскетолазы. Синдром часто встречается у хронических алкоголиков при недостаточном потреблении ими витаминов.
Гипервитаминоз не описан. Избыток принятого витамина быстро выводится с мочой, но у некоторых лиц имеется повышенная чувствительность к парэнтеральному введению препаратов тиамина.
Оценка обеспеченности организма тиамином . С этой целью обычно определяют содержание витамина и/или его коферментов в эритроцитах крови. Поскольку при недостатке витамина В 1 нарушается окислительное декарбоксилирование кетокислот, увеличение содержания в крови и моче пировиноградной и α-кетоглутаровой кислот будет свидетельствовать о недостатке тиамина в организме. Однако следует иметь в виду, что накопление пирувата отмечается не только при гиповитаминозе В 1 , но и при гипоксии и других патологических состояниях.
Наилучшим способом судить о степени обеспеченности организма витамином В 1 является определение активности тиаминзависимых ферментов. Однако активность пируват- и α–кетоглутаратдегидогеназ снижается только при глубоком гиповитаминозе, поскольку их апофермент прочно связывает ТПФ. Транскетолаза связывает ТПФ слабее, и активность ее в эритроцитах начинает снижаться уже на ранних стадиях гиповитаминоза В 1 . Если к образцу крови добавить ТПФ, то величина возрастания активности транскетолазы (так называемый ТПФ-эффект) позволит судить о степени недостаточности тиамина.
Довольно много витамина В 1 содержится в пшеничном хлебе из муки грубого помола, в оболочке семян хлебных злаков, в сое, фасоли, горохе. Много его в дрожжах. Меньше – в картофеле, моркови, капусте. Из продуктов животного происхождения наиболее богаты тиамином печень, нежирная свинина, почки, мозг, яичный желток. В настоящее время дефицит витамина В 1 становится одной из проблем питания, так как из-за высокого потребления сахара и кондитерских изделий, а также белого хлеба и шлифованного риса существенно увеличивается расход этого витамина в организме. Использовать дрожжи в качестве источника витамина не рекомендуется из-за высокого содержания в них пуринов, что может приводить к возникновению обменного артрита (подагры).
Суточная потребность в тиамине – 1,1 –1,5 мг.
Витамин В 2 (рибофлавин)
Химическое строение и свойства . Витамин В 2 отличается от других витаминов желтым цветом (flavus – желтый). Однако в отличие от окисленной желтой, восстановленная форма витамина бесцветная.

Рибофлавин впервые был выделен из кисломолочной сыворотки. Синтезирован Р. Куном в 1935 г. Молекула рибофлавина состоит из гетероциклического изоаллоксазинового ядра, к которому присоединен в 9 положении спирт рибитол (производное D -рибозы). Термином “флавины” обозначаются многие производные изоаллоксазина, обладающие В 2 -витаминной активностью.
Биосинтез флавинов осуществляется растительными и многими бактериальными клетками, а также плесневыми грибками и дрожжами. Благодаря микробному биосинтезу рибофлавина в желудочно-кишечном тракте жвачные животные не нуждаются в этом витамине. У других животных и человека синтезирующихся в кишечнике флавинов недостаточно для предупреждения гиповитаминоза.
Витамин В 2 хорошо растворим в воде, устойчив в кислой среде, но легко разрушается в нейтральной и щелочной, а также под действием видимого и УФ-облучения.
Метаболизм . В пище витамин В 2 находится преимущественно в составе своих коферментных форм, связанных с белками, – флавопротеинов. Под влиянием пищеварительных ферментов витамин высвобождается и всасывается путем простой диффузии в тонком кишечнике. В энтероцитах рибофлавин фосфорилируется до ФМН (флавин-мононуклеотида) и ФАД (флавин-аденин-динуклеотида). Реакции протекают следующим образом:
АТФ Флавокиназа A ДФ
Рибофлавин Рибофлавин-5-фосфат (ФМН)
ФМН связывается с аденозинмонофосфатом при участии фермента пирофосфорилазы.
Пирофосфорилаза
Аналогичные реакции протекают в клетках крови, печени и других тканей.
Биохимические функции . Основное значение витамина В 2 состоит в том, что он входит в состав флавиновых коферментов – ФМН и ФАД. Роль этих коферментов заключается в следующем:
ФМН и ФАД – коферменты оксидаз, переносящих электроны и Н + с окисляемого субстрата на кислород. Таковыми являются ферменты, участвующие в распаде аминокислот (оксидазыD - иL -аминокислот), нуклеотидов (ксантиноксидаза), биогенных аминов (моно- и диаминоксидазы) и др.
ФМН и ФАД – промежуточные переносчики электронов и протонов в дыхательной цепи: ФМН входит в состав I-го коплекса цепи тканевого дыхания, ФАД – в составII-го комплекса.
ФАД – кофермент пируват- и α-кетоглутаратдегидрогеназных комплексов (наряду с ТПФ и другими коферментами ФАД осуществляет окислительное декарбоксилирование соответствующих кетокислот), а также единственный кофермент сукцинатдегидрогеназы (фермента цикла Кребса).
ФАД – участник реакций окисления жирных кислот в митохондриях (он является коферментом ацил-КоА-дегидрогеназы).
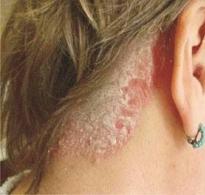
Гиповитаминоз . Недостаток витамина В 2 , как и других витаминов, проявляется слабостью, повышенной утомляемостью и склонностью к простудным заболеваниям. К специфическим проявлениям недостаточности рибофлавина относятся воспалительные процессы в слизистых оболочках. Слизистая губ и полости рта становится сухой, язык приобретает ярко-красный цвет, в углу рта появляются трещины. Отмечается повышенное шелушение эпителия кожи, особенно на лице. Конъюнктива глаза теряет блеск из-за сухости, вызываемой закупоркой слезного канала слущивающимся эпителием. Роговица прорастает сосудами (компенсаторная реакция на недостаточность дыхательной функции роговицы) и затем мутнеет. Отмечается катаракта (помутнение хрусталика).
Гипервитаминоз не описан. При введении больших доз витамина В 2 избыточного накопления флавинов в тканях не происходит, так как рибофлавин быстро выделяется с мочой.
Оценка обеспеченности организма рибофлавином . Содержание витамина В 2 в крови остается в пределах нормы даже при выраженном гиповитаминозе. Смерть наступает еще при достаточном уровне витамина в тканях (30 % от общего количества). О степени тяжести гиповитаминоза следует судить по уровню в тканях его коферментных форм, методы определения которых достаточно трудоемки.
Суточная потребность. Пищевые источники . Суточная потребность в витамине – 1-3 мг.
Основными источниками рибофлавина являются печень, почки, желток куриного яйца, творог. В кислом молоке витамина содержится больше, чем в свежем. В растительных продуктах витамина В 2 мало (исключение – миндальные орехи). Частично дефицит рибофлавина восполняется кишечной микрофлорой.
Хронический недостаток рибофлавина в питании существенно увеличивает риск развития рака пищевода и других органов.
Витамин В1 , был первым витамином, выделенным в кристаллическом виде К. Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название - тиамин - получил из-за наличия в составе его молекулы атома серы и аминогруппы.
Тиамин
состоит из 2-х гетероциклических колец - аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу - карбанион (относительно кислый углерод между серой и азотом).
Тиамин хорошо сохраняется в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде, например при выпечке теста с добавлением соды или карбоната аммония, он быстро разрушается.
В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специфического механизма активного транспорта, остальное его количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и ткани.
Существует мнение, что основной транспортной формой тиамина является ТМФ.
Витамин В1, присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных зфиров: тиаминмонофосфата (ТМФ), тиаминдифосфата (ТДФ, синонимы: тиамин пирофосфат, ТПФ, кокарбоксилаза) и тиаминтрифосфата (ТТФ).
ТТФ - синтезируется в митохондриях с помощью фермента ТПФ-АТФ-фосотрансферазы:
Основной коферментной формой (60-80 % от общего внутриклеточного) является ТПФ. ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия. После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
Витамин В, в форме ТПФ является составной частью ферментов, катализирующих реакции прямого и окислительного декарбоксилирования кетокислот.
Участие ТПФ в реакциях декарбоксилирования кетокислот объясняется необходимостью усиления отрицательного заряда углеродного атома карбонила кетокислоты в переходном, нестабильном, состоянии:
Переходное состояние стабилизируется ТПФ путем делокализаиии отрицательного заряда карбо-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
2. Участие ТПФ в реакциях окислительного декарбоксилирования.
Окислительное декарбоксилирование ПВК катализирует пируватде-гидрогеназа. В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов (см. с. 100). ТПФ катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксила-зой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки - цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплек-са активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.
Окислительное дскарбоксилирование а-кетоглутатарата катализирует а-кетоглутаратдегидрогеназа. Этот фермент является составной частью цикла Кребса. Строение и механизм действия а-кетоглугарат-дегидрогеназного комплекса схожи с пируватдегидрогеназой, т. е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла.
Помимо окислительных превращений ПВК и а-кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвленным углеродным скелетом (продукты дезаминирования ва-лина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.
3. ТПФ - кофермент транскетолазы.
Транскетолаза - фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается в том, что он является основным поставщиком NADFH*H+ и рибозо-5-фосфата. Транскетолаза переносит дву-углеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату,
что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и 7С сахара (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карб-аниона, образующегося при расщеплении связи С2-С3 ксилулозо-5-фосфата.
4. Витамин В1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА - субстрата ацетилирования холина.
5. Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции , конкретный механизм которых еще нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врожденных тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В, как опосредованных стресс-реакцией.
Переходное состояние стабилизируется ТПФ путем дслокализаиии отрицательного заряда карб-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мульти-ферментных комплексов дегидрогеназ а-оксикетокислот (см. ниже).
Министерство здравоохранения Республики Беларусь
Учреждение образования
«Гомельский государственный медицинский университет»
Кафедра_________________________________________________
Обсуждено на заседании кафедры (МК или ЦУНМС)____________________
Протокол № _______
По биологической химии
для студентов_____2-го_____ курса ___лечебного___________________факультета
Тема:___Витамины 2
Время__90 мин___________________
Учебные и воспитательные цели:
Сформировать представление о структуре, метаболизме и молекулярных механизмах действия водорастворимых витаминов. Профилактика гиповитаминозов в состоянии стресса.
1.Водорастворимые
ЛИТЕРАТУРА
1..Основы биохимии:А.Уайт, Ф.Хендлер,Э.Смит, Р.Хилл, И.Леман.-М. книга,
1981,т.3,.с.1703-1757.
2..Питание в профилактике и лечении рака.- Т.С. Морозкина., К.К.Далидович.
Минск., 1998г
3 . .Биохимия человека:, Р.Марри, Д.Греннер, П.Мейес, В.Родуэлл.- М.книга,2004.
4.Наглядная биохимия: Кольман., Рем К.-Г-М.книга 2004г
5. Спиричев
МАТЕРИАЛЬНОЕ ОБЕСПЕЧЕНИЕ
1.Мультимедийная презентация
РАСЧЕТ УЧЕБНОГО ВРЕМЕНИ
Всего: 90 минут
Витамин в1 (Tиамин. Антиневритный витамин)
Химическое строение и свойства . Витамин В 1 был первым витамином, выделенным в кристаллическом виде К. Функом в 1912 г. Позже был осуществлён его химический синтез. Своё название – тиамин – этот витамин получил из-за наличия в составе его молекулы атома серы и амино-группы.
Тиамин состоит из 2-х гетероциклических колец – аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу – карб-анион (относительно кислый углерод между серой и азотом).
Тиамин хорошо сохраняется в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде, например при выпечке теста с добавлением соды или карбоната аммония, он быстро разрушается.
Метаболизм . В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специфического механизма активного транспорта, остальное его количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и ткани.
ТПФ-киназа
АТФ + тиамин тиаминпирофосфат + АМФ
Существует мнение, что основной транспортной формой тиамина является ТМФ.
В итамин
В 1
присутствует в различных органах и
тканях как в форме свободного тиамина,
так и его фосфорных эфиров: тиаминмонофосфата
(ТМФ), тиаминдифосфата (ТДФ, синонимы:
тиаминпирофосфат, ТПФ, кокарбоксилаз
а)
и тиаминтрифосфата (ТТФ).
итамин
В 1
присутствует в различных органах и
тканях как в форме свободного тиамина,
так и его фосфорных эфиров: тиаминмонофосфата
(ТМФ), тиаминдифосфата (ТДФ, синонимы:
тиаминпирофосфат, ТПФ, кокарбоксилаз
а)
и тиаминтрифосфата (ТТФ).
ТТФ – синтезируется в митохондриях с помощью фермента ТПФ-АТФ-фосфотрансферазы:
трансфереза
ТПФ + АТФ ТДФ + АМФ
Основной коферментной формой (60-80% от общего внутриклеточного содержания) является ТПФ.
ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия.
После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
Биохимические функции . Витамин В 1 в форме ТПФ является составной частью ферментов, катализирующих реакции прямого и окислительного декарбоксилирования кетокислот.
Участие ТПФ в реакциях декарбоксилирования кетокислот объясняется необходимостью усиления отрицательного заряда углеродного атома карбонила кетокислоты в переходном, нестабильном, состоянии:
О – С – C = O CO 2 + - C = O
Кетокислота переходное состояние
Переходное состояние стабилизируется ТПФ путём делокализации отрицательного заряда карб-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с лёгкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мультиферментных комплексов дегидрогеназ α-оксикетокислот (см. ниже).
пировиноградной кислоты (ПВК).
1 .
Участие ТПФ в реакции прямого
декарбоксилирования пировиноградной
кислоты (ПВК).
При
декарбоксилировании ПВК с помощью
пируватдекарбоксилазы образуется
ацетальдегид, который под воздействием
алкогольдегидрогеназы превращается в
этанол.ТПФ является незаменимым
кофактором пируватдекарбоксилазы. Этим
ферментом богаты дрожжи.
.
Участие ТПФ в реакции прямого
декарбоксилирования пировиноградной
кислоты (ПВК).
При
декарбоксилировании ПВК с помощью
пируватдекарбоксилазы образуется
ацетальдегид, который под воздействием
алкогольдегидрогеназы превращается в
этанол.ТПФ является незаменимым
кофактором пируватдекарбоксилазы. Этим
ферментом богаты дрожжи.
Окислительное декарбоксилирование ПВК катализирует пируватдегидрогеназа . В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов (см.гл.) ТПФ катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксилазой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки – цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплекса активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.
Окислительное декарбоксилирование α-кетоглутатарата катализирует α –кетоглута-ратдегидрогеназа . Этот фермент является составной частью цикла Кребса. Строение и механизм действия α-кетоглутаратдегидрогеназного комплекса схожи с пируватдегидрогеназой, т.е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла.
Помимо окислительных превращений ПВК и α-кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвлённым углеродным скелетом (продукты дезаминирования валина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.
3. ТПФ – кофермент транскетолазы . Транскетолаза – фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается в том, что он является основным поставщиком НАДФH . H + и рибозо-5-фосфата. Транскетолаза переносит двууглеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату, что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и 7 С сахара (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карб-аниона, образующегося при расщеплении связи С2- С3 ксилулозо-5-фосфата.
4 . Витамин В 1 принимает участие в синтезе ацетилхолина , катализируя в пируватдегидрогеназной реакции образование ацетил-КоА – субстрата ацетилирования холина.
5. Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции , конкретный механизм которых ещё нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врождённых тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В 1 как опосредованных стресс-реакцией.
Гиповитаминоз. Уже ранние проявления гиповитаминоза сопровождаются снижением аппетита и тошнотой. Отмечаются неврологические расстройства, к которым относятся нарушение периферической чувствительности, ощущение ползания «мурашек», невралгии. Характерна забывчивость, особенно на недавние события. Слабость сердечной мышцы проявляется тахикардией даже при незначительных нагрузках.
Недостаток в пище тиамина приводит к значительному накоплению пировиноградной и α-кетоглутаровой кислот, снижению активности тиаминзависимых ферментов в крови и тканях организма.
В эксперименте показано, что тиаминовая недостаточность сопровождается нарушением структуры и функции митохондрий. Добавление к последним ТПФ нормализует тканевое дыхание. У белых крыс, лишенных таимина, развивалась анорексия, уменьшалась масса тела. Шерсть теряла свой блеск, становилась взъерошенной. Животные мало двигались и обычно лежали, свернувшись в углу клетки. Анорексия является результатом резкого угнетения секреции желудочного сока и ослаблением его переваривающей способности.
Алиментарная недостаточность тиамина у человека приводит к патологическим изменениям в нервной, сердечно-сосудистой и пищеварительной системах, сопровождаясь общим истощением организма.
Болезнь «бери-бери» возникает при значительном дефиците тиамина и характеризуется крайне тяжёлым течением. В прошлом веке в странах Востока унесла миллионы жизней. «Бери-бери» в переводе с индийского означает «овца». Походка больного, действительно, похожа на поступь овцы (симптом симметричного опускания стоп). Поскольку у заболевших отмечалась тяжесть в ногах и скованность походки, «бери-бери» называлась также «кандальной болезнью». Этим заболеванием часто страдали заключённые, рацион питания которых состоял в основном из очищенного риса. Проявление недостаточности тиамина можно наблюдать до сих пор у бедных лиц в тех странах, где основу питания населения составляет полированный рис – в шлифованном зерне, в отличие от неочищенного, нет этого витамина. Последняя эпидемия «бери-бери» была на Филиппинах в 1953 г (погибло 100 000 человек).
Болезнь имеет 2 формы: сухую (нервно-паралитическую) и отёчную (сердечную). Причем в обоих случаях поражаются и сердечно-сосудистая и нервная системы, но в разной степени. В настоящее время классической «бери-бери», по-видимому, уже нет, однако явления умеренного гиповитаминоза отмечаются часто. К основным симптомам недостаточности тиамина относятся: физическая слабость, снижение аппетита (витамин В 1 необходим для стимуляции желудочной секреции), стойкие запоры; расстройство функции нервной системы (онемение пальцев, чувство «ползания мурашек», утрата периферических рефлексов, боль по ходу нервов); нарушения психической деятельности (раздражительность, забывчивость, страх, иногда галлюцинации, снижение интеллекта). Позже развивается глубокое поражение нервной системы, характеризующееся потерей чувствительности конечностей, развитием параличей, атрофией мышц в результате нарушения их иннервации. При отёчной форме, наряду с явлениями полиневрита, отмечаются тахикардия и одышка даже при незначительных нагрузках. Из-за слабости сердечной мышцы развиваются отёки. Особенно часто проявления тиаминовой недостаточности наблюдаются у хронических алкоголиков вследствие их склонности больше пить, чем есть. Синдром Вернике, развивающийся у этих лиц, характеризуется нарушением координации движений, зрительной функции, спутанностью сознания.
Особая чувствительность нервной ткани к недостатку тиамина объясняется тем, что коферментная форма этого витамина абсолютно необходима нервным клеткам для усвоения глюкозы, которая является для них почти единственным источником энергии (большинство других клеток организма может использовать иные энергетические вещества, например жирные кислоты). Кстати, питание преимущественно углеводной пищей (белый хлеб, сладости) приводит к повышенной потребности в тиамине и, следовательно, развитию вторичной тиаминовой недостаточности.
Врождённые нарушения обмена тиамина .
Синдром Wernicke -К orsakoff . В основе этого синдрома, сопровождающегося потерей памяти и частичным параличом, лежит изменение свойств фермента транскетолазы, у которой уменьшается сродство к ТПФ. Гены других ТПФ-зависимых ферментов не затрагиваются. Заболевание проявляется, если уровень потребляемого ТПФ снижается ниже значений, необходимых для насыщения транскетолазы. Синдром часто встречается у хронических алкоголиков при недостаточном потреблении ими витаминов.
Перемежающаяся атаксия . Заболевание обусловлено врождённым дефектом пируватдегидрогеназы.
Тиаминзависимая форма болезни «моча с запахом кленового сиропа ». При этой патологии отмечается дефект окислительного декарбоксилирования разветвлённых кетокислот. В крови и моче резко увеличивается содержание разветвлённых кетокислот (отсюда – специфический запах мочи) и их субстратов – аминокислот валина, изолейцина и лейцина. Клиническая симптоматика схожа с терминальной стадией В 1 -недостаточности.
Подострая некротизирующая энцефалопатия . При этом заболевании нарушается образование ТТФ в мозге. Энцефалопатия проявляется в потере аппетита, рвоте, затруднении сосания. Младенцы теряют способность держать головку, у них отмечаются многочисленные неврологические расстройства. Болезнь заканчивается без лечения летально в течение первых лет жизни.
Тиаминзависимая мегалобластическая анемия . Механизм участия тиамина в кроветворении до конца не выяснен.
Гипервитаминоз не описан. Избыток принятого витамина быстро выводится с мочой, но у некоторых лиц имеется повышенная чувствительность к парэнтеральному введению препаратов тиамина.
Оценка обеспеченности организма тиамином . С этой целью обычно определяют содержание витамина и/или его коферментов в эритроцитах крови. Поскольку при недостатке витамина В 1 нарушается окислительное декарбоксилирование кетокислот, увеличение содержания в крови и моче пировиноградной и α-кетоглутаровой кислот будет свидетельствовать о недостатке тиамина в организме. Однако следует иметь в виду, что накопление пирувата отмечается не только при гиповитаминозе В 1 , но и при гипоксии и других патологических состояниях.
Наилучшим способом судить о степени обеспеченности организма витамином В 1 является определение активности тиаминзависимых ферментов. Однако активность пируват- и α–кетоглутаратдегидогеназ снижается только при глубоком гиповитаминозе, поскольку их апофермент прочно связывает ТПФ. Транскетолаза связывает ТПФ слабее и активность её в эритроцитах начинает снижаться уже на ранних стадиях гиповитаминоза В 1 . Если к образцу крови добавить ТПФ, то величина возрастания активности транскетолазы (так называемый ТПФ-эффект) позволит судить о степени недостаточности тиамина.
Суточная потребность. Пищевые источники .
Довольно много витамина В 1 содержится в пшеничном хлебе из муки грубого помола, в оболочке семян хлебных злаков, в сое, фасоли, горохе. Много его в дрожжах. Меньше – в картофеле, моркови, капусте. Из продуктов животного происхождения наиболее богаты тиамином печень, нежирная свинина, почки, мозг, яичный желток. В настоящее время дефицит витамина В 1 становится одной из проблем питания, так как из-за высокого потребления сахара и кондитерских изделий, а также белого хлеба и шлифованного риса существенно увеличивается расход этого витамина в организме. Использовать дрожжи в качестве источника витамина не рекомендуется из-за высокого содержания в них пуринов, что может приводить к возникновению обменного артрита (подагры).
Суточная потребность в тиамине – 1,1-1,5 мг.
| Раздел 11.1 |
Понятие о полноценном пищевом рационе. |
|
11.1.1. Полноценным называется рацион, соответствующий энергетическим потребностям человека и содержащий необходимое количество незаменимых пищевых веществ, обеспечивающих нормальный рост и развитие организма. Факторы, влияющие на потребность организма в энергии и питательных веществах: пол, возраст и масса тела человека, его физическая активность, климатические условия, биохимические, иммунологические и морфологические особенности организма. Все питательные вещества можно разделить на пять классов: 1. белки; 2. жиры; 3. углеводы; 4. витамины; 5. минеральные вещества. Кроме того, любая диета должна содержать воду, как универсальный растворитель. Незаменимыми компонентами пищевого рациона являются:
11.1.2. Сбалансированный пищевой рацион. Диета, содержащая питательные вещества в соотношении, оптимальном для максимального удовлетворения пластических и энергетических потребностей организма человека, называется сбалансированным пищевым рационом. Считается, что самым благоприятным является соотношение белков, жиров и углеводов близкое к 1:1:4, при условии что общая калорийность рациона соответствует энергозатратам данного человека. Так, для студента-юноши весом 60 кг, энергозатраты составляют в среднем 2900 ккал в сутки и рацион должен содержать: 80-100 г белков, 90 г жиров, 300 - 400 г углеводов. |
|
| Раздел 11.2 | Характеристика пищевых белков. |
|
11.2.1. Биологическая роль пищевых белков заключается в том, что они служат источником незаменимых и заменимых аминокислот. Аминокислоты используются организмом для синтеза собственных белков; в качестве предшественников небелковых азотистых веществ (гормонов, пуринов, порфиринов и др.); как источник энергии (окисление 1 г белков даёт примерно 4 ккал энергии). Пищевые белки делятся на полноценные и неполноценные. Полноценные пищевые белки - животного происхождения, содержат в своём составе все аминокислоты в необходимых пропорциях и хорошо усваиваются организмом. Неполноценные белки - растительного происхождения, не содержат, или содержат в недостаточном количестве одну или несколько незаменимых аминокислот. Так, зерновые культуры, дефицитны по лизину, метионину, треонину; в белке картофеля мало метионина и цистеина. Для получения полноценных по белку пищевых рационов, следует комбинировать растительные белки, дополняющие друг друга по аминокислотному составу, например, кукурузу и бобы. Суточная потребность: не менее 50 г в сутки, в среднем 80-100 г. 11.2.2. Белковая недостаточность в детском возрасте вызывает: 1. снижение сопротивляемости организма инфекциям; 2. остановку роста вследствие нарушения синтеза факторов роста; 3. энергетическую недостаточность организма (истощение углеводных и жировых депо, катаболизм тканевых белков); 4. потерю массы тела - гипотрофию. При белковом голодании наблюдаются отеки, которые возникают вследствие снижения содержания белков в крови (гипоальбуминемии ) и нарушения распределения воды между кровью и тканями. |
|
| Раздел 11.3 | Характеристика пищевых жиров. |
|
11.3.1. В состав пищевых жиров входят в, основном, триацилглицеролы (98%), фосфолипиды и холестерол. Триацилглицеролы животного происхождения содержат много насыщенных жирных кислот и имеют твёрдую консистенцию. Растительные жиры содержат больше ненасыщенных жирных кислот и имеют жидкую консистенцию (масла). Биологическая роль: 1. являются одним из основных источников энергии; 2. служат источником незаменимых полиненасыщенных жирных кислот; 3. способствуют всасыванию из кишечника жирорастворимых витаминов. Полиненасыщенные жирные кислоты необходимы организму для построения фосфолипидов, формирующих основу всех мембранных структур клетки и липопротеинов крови. Кроме того, линолевая кислота используется для синтеза арахидоновой кислоты, служащей предшественником простагландинов, простациклинов, тромбоксанов и лейкотриенов. Суточная потребность: 90-100 г, из них 30% должны приходиться на растительные масла. Пищевая ценность растительных жиров выше, чем животных, так как при равном энергетическом эффекте - 9 ккал на 1 г, они содержат больше незаменимых жирных кислот. 11.3.2. Нарушение соотношения доли растительных и животных жиров в рационе приводит к изменению соотношения в крови различных классов липопротеинов и, как следствие, к ишемической болезни сердца и атеросклерозу. |
|
| Раздел 11.4 |
Характеристика пищевых углеводов. |
|
11.4.1. Пищевые углеводы по способности усваиваться организмом человека делятся на две группы: усвояемые: глюкоза, фруктоза, сахароза, лактоза, крахмал; неусвояемые: целлюлоза (клетчатка), гемицеллюлоза, пектины. Биологическая роль усвояемых углеводов: 1. являются основным источником энергии для человека (окисление 1 г дает 4 ккал); 2. служат предшественниками в синтезе многих биомолекул - гетерополисахаридов, гликолипидов, нуклеиновых кислот. Биологическая роль неусвояемых углеводов: клетчатка влияет на перистальтику кишечника, способствует выведению холестерола, препятствует развитию ожирения и желчнокаменной болезни. Суточная потребность: 300-400 г, из них - легкоусвояемых углеводов (фруктозы, сахарозы, лактозы) - 50-100 г, клетчатки 25 г, остальное - крахмал. 11.4.2. Избыток легкоусвояемых углеводов в рационе способствует развитию таких заболеваний как ожирение, сахарный диабет, кариес зубов. Недостаток балластных веществ (клетчатки) способствует развитию рака толстой кишки. |
|
| Раздел 11.5 |
Витамины. |
||||||||||||||||||||||||
|
11.5.1. Витамины - низкомолекулярные органические соединения, поступающие в организм с пищей и обеспечивающие нормальное протекание биохимических и физиологических процессов. Витамины не включаются в структуру тканей и не используются в качестве источника энергии. 11.5.2. Классификация витаминов. Витамины делятся на две группы: витамины, растворимые в воде и витамины, растворимые в жирах. Водорастворимые витамины - В1, В2 , В6 , В12 , РР, Н, С, фолиевая кислота, пантотеновая кислота. Жирорастворимые витамины - А, Д, Е, К. Для каждого витамина, кроме буквенного обозначения, существует химическое и физиологическое название. Физиологическое название, как правило, состоит из приставки анти- и названия заболевания, развитие которого предупреждает витамин (например, витамин Н - антисеборрейный). 11.5.3. Провитамины. Некоторые витамины могут синтезироваться непосредственно в организме человека. Соединения, служащие предшественниками для синтеза витаминов в клетках организма человека, называются провитаминами . Например, провитамином витамина А является каротин, витамина D2 - эргостерол, D3 - 7-дегидрохолестерол. 11.5.4. Биологическая роль витаминов. Витамины, попадая в организм, превращаются в свою активную форму, которая и принимает непосредственное участие в биохимических процессах.Биологическая роль водорастворимых витаминов заключается в том, что они входят в состав коферментов , участвующих в метаболизме белков, жиров и углеводов в клетках организма человека. В таблице 1 приведены примеры витаминов и их биологическая роль. Таблица 1. Коферментные функции водорастворимых витаминов.
11.5.5. Антивитамины. Термином антивитамины обозначают любые вещества, вызывающие снижение или полную потерю биологической активности витаминов. По механизму действия их делят на две группы: 1. антивитамины, имеющие структуру, сходную со строением витамина и конкурирующие с ним за включение в кофермент; 2. антивитамины, вызывающие химическую модификацию витамина. Примерами могут служить: тиаминаза (антивитамин В1 ), акрихин (антивитамин В2 ), изониазид (антивитамин РР), дикумарол (антивитамин К). 11.5.6. Болезни нерационального потребления витаминов. Для обеспечения нормального протекания биохимических процессов, в организме человека должен поддерживаться определённый уровень концентрации витаминов. При изменении этого уровня развиваются заболевания с симптомами, харктерными для каждого витамина. Гипервитаминозы - заболевания, вызванные избыточным содержанием витаминов в организме. Характерны для жирорастворимых витаминов, способных накапливаться в клетках печени. Чаще всего встречаются гипервитаминозы А и D, связанные с передозировкой их лекарственных препаратов. Гипервитаминоз А характеризуется общими симптомами отравления: сильными головными болями, тошнотой, слабостью. Гипервитаминоз D сопровождается деминерализацией костей, кальцинацией мягких тканей, образованием камней в почках. Гиповитаминозы - заболевания , вызванные недостатком витаминов в организме. Первичные гиповитаминозы связаны с нарушением процессов поступления витаминов в организм при: 1. недостатке витаминов в пище; 2. ускоренном распаде витаминов в кишечнике под действием патогенной микрофлоры; 3. нарушении синтеза витаминов кишечной микрофлорой при дисбактериозе; 4. нарушении всасывания витаминов; 5. приеме лекарственных препаратов - антивитаминов. Вторичные гиповитаминозы связаны с нарушением процессов превращения витаминов в их активные формы в клетках организма человека. Причиной могут служить генетические дефекты или нарушения биохимических процессов при различных заболеваниях органов и тканей. Авитаминозы - заболевания , вызванные полным отсутствием витамина в организме. |
|||||||||||||||||||||||||
| Раздел 11.5.5 |
Строение и биологические функции жирорастворимых витаминов. |
|
Витамин А - ретинол. Активная форма:
цис-ретиналь. Участие витамина А в механизме сумеречного зрения. В процессе светоощущения главная роль принадлежит пигменту родопсину - сложному белку, состоящему из белка опсина и простетическойгруппы - цис-ретиналя . Под действием света цис-ретиналь света превращается в изомер - транс-ретиналь, что приводит к разрушению пигмента родопсина и возникновению нервного импульса. Восстановление пигмента происходит по схеме: Процесс изомеризации транс-ретинола в сетчатке глаза протекает очень медленно. Основное его количество поступает в кровь, затем в печень, где и происходит быстрое превращение транс-ретинола в цис-ретинол, который попадает в кровь и поглощается сетчаткой глаза. Процесс лимитируется запасом в печени транс-ретинола (витамина А). Гиповитаминоз: нарушение темновой адаптации зрения (ночная слепота) у взрослых; у детей - остановка роста, ороговение эпителия всех органов - гиперкератоз , сухость роговицы глаза - ксерофтальмия , размягчение роговицы под действием микрофлоры - кератомаляция . Витамин D 3 - холекальциферол. Активная форма:
1,25-дигидроксихолекальциферол, кальцитриол. Синтез витамина D3 и его активных форм в тканях человека. Предшественником (провитамином) витамина D3 в организме человека служит 7-дегидрохолестерол, который при действиина кожу ультрафиолетового излучения, переходит в холекальциферол.
Образование активной формы витамина происходит последовательно в печени и почках путём гидроксилирования по 1 и 25 углеродным атомам . Образующийся 1,25-дигидроксихолекальциферол обладает гормональной активностью (кальцитриол). Тканями-мишенями для него являются кишечник, почки, кости. В эпителии кишечника и почечных канальцах кальцитриол индуцирует синтез Са-связывающего белка, что способствует всасыванию ионов Са2+ из пищи и реабсорбции их почками. В костной ткани угнетает синтез коллагена, уменьшает Са- связывающую способность, что приводит к мобилизации кальция из костей. Гиповитаминоз:
у детей - рахит
. Симптомы: 1. снижение мышечного тонуса; 2. деформация костей черепа, груди, позвоночника, нижних конечностей. У взрослых - остеопороз
- деминерализация костей.
Витамин К - филлохинон. Активная форма:
неизвестна. Витамин Е - токоферол. Активная форма:
неизвестна. |
|
| Раздел 11.5. 6 |
Строение и биологические функции водорастворимых витаминов. |
|
Витамин В1 - тиамин.
Биологическая роль: участвует в реакциях окислительного декарбоксилирования пирувата и α-кетоглутарата. Суточная потребность: 1-2 мг. Основные пищевые источники: мука грубого помола, бобовые, мясо, рыба. Гиповитаминоз: болезнь “бери-бери” . Симптомы: 1. периферические невриты; 2. мышечная слабость; 3. дискоординация движений; 4. увеличение размеров сердца; 5. повышение уровня пирувата в крови. Основная причина смертности у больных бери-бери - сердечная недостаточность. Витамин В2 - рибофлавин.
Биологическая роль: участвует в окислительно-восстановительных реакциях. Например: 1. перенос электронов в дыхательной и монооксигеназной цепях; 2. окисление сукцината; 3. окисление высших жирных кислот. Суточная потребность: 1,5 - 3,0 мг. Основные пищевые источники: молоко, печень, мясо, яйца, жёлтые овощи. Гиповитаминоз часто встречается у беременных, детей, у людей в состоянии стресса. Симптомы: 1. воспаление сосочков языка -глоссит ; 2. растрескивание губ и уголков рта - ангулярный стоматит ; 3. помутнение хрусталика - катаракта ; 4. воспаление роговицы глаза - кератит . Витамин В6 - пиридоксин.
Биологическая роль: - участвует в реакциях: 1. трансаминирования; 2. Декарбоксилирования аминокислот; 3. синтеза никотинамида из триптофана; 4. синтеза δ-аминолевулиновой кислоты (синтез гема). Суточная потребность: 2 мг. Основные пищевые источники: хлеб, горох, фасоль, картофель, мясо. Гиповитаминоз: недостаточность витамина не вызывает специфических симптомов. Витамин РР - никотинамид (ниацин).
Биологическая роль: входит в состав дегидрогеназ. Например: 1. пируватдегидрогеназный комплекс; 2. глюкозо-6-фосфатдегидрогеназа; 3. глутаматдегидрогеназа; 4. β-гидрокси,β-метилглутарил-КоА-редуктаза и многие другие. Суточная потребность: 15 - 20 мг. Основные пищевые источники: мясо, рыба,горох, бобы, орехи. Гиповитаминоз: болезнь пеллагра . Симптомы: 1. дерматит - поражение кожи; 2. диаррея - поражение слизистой желудочно-кишечного тракта; 3. деменция - слабоумие. Поскольку витамин РР может синтезироваться в организме из аминокислоты триптофан, пеллагру можно лечить, вводя в диету дополнительное количество полноценных животных белков. 60 мг триптофана эквивалентны 1 мг никотинамида. Витамин В9 - фолиевая кислота .
Биологическая роль: участвует в реакциях переноса одноуглеродных групп при синтезе: 1. пуриновых нуклеотидов; 2. тимидилового нуклеотида; 3. метионина из гомоцистеина; 4. серина и глицина. Суточная потребность: 1 - 2,2 мг. Основные пищевые источники: зелёные листья растений, дрожжи. Гиповитаминоз: макроцитарная анемия. Витамин В12 - цианкобаламин . Активная форма: коферменты метилкобаламин и дезоксиаденозилкобаламин. Имеют сложную структуру, в центре которой находится атом кобальта (Со+ ), соединённый с четырьмя пиррольными кольцами, образующими корриновое ядро . Биологическая роль: участвует в реакциях: 1. трансметилирования; 2. обмена серосодержащих аминокислот; 3. образования коферментных форм фолиевой кислоты. Суточная потребность: 0,003 мг. Основные пищевые источники: любые продукты животного происхождения. Гиповитаминоз : мегалобластическая анемия , развивающаяся при нарушении всасывания витамина в кишечнике. Для всасывания витамина В12 в кишечнике, необходим специальный белокгастромукопротеин (транскоррин), получивший название - внутренний фактор Касла . Этот белок вырабатывается в желудке, связывает витамин В12 (внешний фактор Касла) и образовавшийся комплекс всасывается в кишечнике. Любые причины, приводящие к нарушению выработки желудочного гликопротеина (например, органические поражения желудка, резекция желудка) приводят к гиповитаминозу В12 . Витамин С - аскорбиновая кислота.
Активная форма
- неизвестна. Витамин Н - биотин.
Активная форма: биоцитин. Биологическая роль - участвует в реакциях карбоксилирования при синтезе: 1. пуриновых нуклеотидов; 2. оксалоацетата; 3. малонил-КоА. Суточная потребность: 0,26 мг. Основные пищевые источники: молоко, яичный желток, печень, томаты, шпинат. Гиповитаминоз: так как витамин синтезируется микрофлорой кишечника, то недостаточность встречается редко. Проявляется в виде специфических дерматитов волосистой части |
|
| Раздел 11.6 |
Минеральные (неорганические) вещества. |
|
11.6.1. Кроме шести главных элементов - С, Н, О, Р, N, S, из которых состоят все органические молекулы, человеку необходимо получать ещё около 20 химических элементов. В зависимости от количества, в каком они должны поступать в организм, минеральные вещества делятся на: макроэлементы - кальций, хлор, магний, калий, натрий - суточная потребность более 100 мг имикроэлементы - железо, марганец, медь, йод, фтор, молибден, селен, цинк и др. - суточная потребность - несколько миллиграммов. 11.6.2. Биологическая роль минеральных веществ: 1. являются структурными компонентами тканей (кальций, фтор); 2. обеспечивают водно-солевой баланс (натрий, калий); 3. являются простетической группой ферментов, входят в состав активных центров, стабилизируют структуру ферментов и фермент-субстратных комплексов (магний, железо, медь); 4. участвуют в передаче нервных импульсов (кальций); 5. участвуют в гормональной регуляции обмена веществ (иод входит в состав гормонов щитовидной железы, цинк - в состав инсулина). 11.6.3. Дефицит микроэлементов в воде и пище может приводить к развитию заболеваний. Например, недостаток железа и меди может вызывать анемию, недостаток фтора способствовать возникновению кариеса, при нехватке йода в пище и воде развивается эндемический зоб. |
|
| Раздел 11.7 |
Химические и биологические загрязнители пищи. |
|
11.7.1. Химические загрязнители пищи - продукты технологической деятельности человека. Они попадают в организм с растительной пищей, молоком и мясом животных, выращенных в экологически неблагополучных регионах, а также с консервированными продуктами, приготовленными с нарушением технологии. К химическим загрязнителям относят 1. радиоактивные изотопы; 2. ионы тяжёлых металлов; 3. органические продукты химической промышленности; 4. сельскохозяйственные яды; 5. пищевые добавки. Большинство химических загрязнителей могут накапливаться в организме человека и нарушать обмен веществ. Ионы тяжёлых металлов : ртуть, свинец, медь, олово, цинк, железо - взаимодействуют с атомами азота нуклеиновых кислот и серы в составе белков, вызывают нарушение функционирования этих макромолекул. При отравлении свинцом отмечаются повышенная утомляемость, бессонница, позднее - расстройства нервной системы, поражение головного мозга. У детей накопление свинца в тканях вызывает снижение умственных способностей. Нитраты попадают в организм с растительной пищей и водой, в кишечнике восстанавливаются до нитритов , которые окисляют гемоглобин (Fe2+ ) в метгемоглобин (Fe3+ ). При отравлении нитритами появляются одышка, головокружение, цианоз , метгемоглобинемия . Кроме того, нитриты, взаимодействуют с аминами (содержащимися в продуктах) образуют нитрозамины - вещества, вызывающие возникновение мутаций и развитие раковых опухолей. Фенолы , содержащиеся в стоках металлургических предприятий, в питьевой воде в присутствии хлора и на свету способны превращаться в диоксины. Это липофильные соединения, легко встраивающиеся в клеточные мембраны, поражают иммунокомпетентные клетки, вызывают врожденные уродства у детей и опухолевые заболевания. 11.7.2. Биологические загрязнители пищи: токсичные вещества, продуцируемые бактериями, низшими грибами, одноклеточными водорослями; биологически активные соединения, содержащиеся в высших растениях. Микотоксины - продуцируются микроскопическими грибами - плесенью. Многие из этих веществ способны накапливаться в организме и вызывать при этом эмбриотоксический, мутагенный и канцерогенный эффекты. Например, афлатоксин , вырабатывается грибками, поражающими арахис и кукурузу, является сильнейшим печеночным ядом с выраженным канцерогенным эффектом. Альготоксины - синтезируются низшими водорослями. Отравление происходит при купании в водоёмах, зараженных такими водорослями, и поедании обитающей в них рыбы. Например,анатоксин , вызывает блокирование нервно-мышечной передачи, что приводит к параличу скелетной и дыхательной мускулатуры. Растительные гликозиды - могут содержаться в продуктах в дозах, сопоставимых с фармакологическими. Соланин - образуется в клубнях картофеля под действием солнечного света. Он обладает раздражающим действием на слизистые, угнетает деятельность центральной нервной системы. |
|
Витамины. История букв с цифрами, или Что такое провитамин В5
А.Е. Любарев
Так получилось, что терминология витаминов довольно запутана. Многие, наверное, задумывались: почему есть витамины В6 и В12 , но ничего не слышно про витамины В4 , В7 , В8 , В10 и В11 ? Почему есть витамины К и Р, но не известен, скажем, витамин L или N? Самый простой ответ - так сложилось исторически. Но можно попробовать разобраться, почему же сложилось именно так.
Открытие витаминов
Впервые вывод о существовании неизвестных веществ, абсолютно необходимых для жизни, сделал Николай Лунин в 1880 г. В своей диссертационной (по современным меркам - дипломной) работе, выполненной в Дерптском (ныне Тартуском) университете, он обнаружил, что мыши не могут выжить, питаясь искусственной смесью из белка, жира, сахара и минеральных солей.
Вывод Лунина не получил признания, даже его руководитель Г.Бунге отнесся к этой идее скептически. И его можно понять. Еще в XIV в. английский философ Уильям Оккам провозгласил: "Сущности не следует умножать без необходимости". И этот принцип, известный как "бритва Оккама", ученые взяли на вооружение.
Вот и в случае с открытием Лунина научный мир не спешил признавать существование каких-то неизвестных веществ. Ученые вначале хотели убедиться в том, что смерть мышей не обусловлена нехваткой веществ уже известных. Предположений было много: нарушение "нормального соединения органических и неорганических частей", неравноценность молочного и тростникового сахара, недостаток органических соединений фосфора и т.п.
И все-таки Лунин оказался прав! Его работа не была забыта, напротив, она стимулировала дальнейшие исследования в этом направлении. Но уровень экспериментального мастерства Лунина долгое время не был превзойден. Его последователи часто получали ошибочные результаты вследствие либо недостаточной очистки веществ, либо копрофагии (поедание собственного кала), либо недостаточной продолжительности опытов.
Каждая мелочь имела значение. Например, Лунин брал не молочный, а тростниковый сахар. Критики обращали на это внимание: искусственная смесь Лунина не совсем адекватна молоку. Но те, кто использовал молочный сахар, не учитывали, что он недостаточно очищен: впоследствии выяснилось, что в нем содержатся в виде примеси витамины группы В.
Потребовалось тридцать лет для того, чтобы убедиться, что неудачи в кормлении животных искусственными смесями не связаны с отсутствием в пище ни нуклеиновых кислот, ни фосфолипидов, ни холестерина, ни незаменимых аминокислот, ни органических комплексов железа. И вывод о том, что в продуктах питания содержатся в очень малых количествах вещества, абсолютно необходимые для жизни, становился все более очевидным.
В то время медики пытались понять причины таких распространенных заболеваний, как цинга, бери-бери и пеллагра. Неоднократно высказывались предположения, что эти болезни связаны с неполноценным питанием, но доказать эту точку зрения было невозможно без экспериментальной проверки на животных.
В 1889 г. голландский врач Х.Эйкман обнаружил у кур заболевание, сходное с бери-бери. Болезнь вызывалась при питании полированным рисом. Через несколько лет норвежские ученые сумели вызвать у морских свинок экспериментальную цингу и показать, что она также связана с недостатком питания.
К 1910 г. был накоплен достаточный материал для открытия витаминов. И в 1911-1913 гг. произошел прорыв в этом направлении. За очень короткое время появилось большое число работ, заложивших основы учения о витаминах.
В 1910 г. директор Листеровского института в Лондоне Ч.Дж. Мартин поручил молодому поляку К.Функу заняться выделением вещества, которое предотвращает от бери-бери. Мартин полагал, что это - какая-то незаменимая аминокислота. Но Функ, проанализировав литературу и проделав ряд предварительных опытов, пришел к выводу, что активным веществом является простое азотсодержащее органическое основание (амин), и применил методы исследования, разработанные для таких соединений.
В 1911 г. Функ сделал первое сообщение о выделении кристаллического активного вещества из рисовых отрубей. Затем он получил аналогичный препарат также из дрожжей и некоторых других источников. Год спустя подобный препарат получили и японские ученые. Как выяснилось впоследствии, эти препараты не были индивидуальным химическим веществом, но проявляли активность на голубях в дозах 4-5 мг.
Функ назвал открытое им вещество "витамин" (vitamine ): от латинского vita - жизнь и "амин" (amine ) - класс химических соединений, к которому принадлежит это вещество. Большая заслуга Функа состоит также в том, что он обобщил данные по таким болезням, как бери-бери, цинга, пеллагра и рахит, и заявил, что каждая из этих болезней вызывается отсутствием специфического вещества. Он считал, что эти вещества составляют особую химическую группу азотистых соединений, поэтому дал им всем обобщающее название "витамины". Статья Функа под названием "Этиология болезней недостаточности" (The etiology of the deficiency diseases ) вышла в июне 1912 г. Два года спустя Функ издал монографию под названием "Витамины".
Почти одновременно с вышеупомянутой статьей Функа, в июле 1912 г., была опубликована большая работа известного английского биохимика Ф.Г. Хопкинса. В тщательно проведенном эксперименте на крысах он доказал, что для роста животных необходимы вещества, присутствующие в молоке в небольших количествах, при этом их действие не связано с улучшением усвояемости основных компонентов пищи, т.е. они имеют самостоятельное значение. Функ знал о работе Хопкинса еще до выхода этой статьи, в своей статье он предполагал, что открытые Хопкинсом факторы роста также являются витаминами.
Дальнейшие успехи в развитии учения о витаминах связаны в первую очередь с работами двух групп американских ученых: Т.Б. Осборна-Л.В. Менделя и Э.В. Мак-Коллума-М.Дэвис. В 1913 г. обе группы пришли к выводу, что в некоторых жирах (молочном, рыбьем, жире яичного желтка) содержится фактор, необходимый для роста. Два года спустя, под влиянием работ Функа и Хопкинса и избавившись от экспериментальных ошибок, они убедились в существовании еще одного фактора - водорастворимого. Жирорастворимый фактор не содержал азот, поэтому Мак-Коллум не стал использовать термин "витамин". Он предложил называть активные вещества "жирорастворимый фактор А" и "водорастворимый фактор В".
Вскоре выяснилось, что "фактор В" и препарат, полученный Функом, взаимозаменяемы, а "фактор А" предотвращает ксерофтальмию и рахит. Родство витаминов и факторов роста стало очевидным. Был получен еще один фактор - противоцинготный. Возникла необходимость упорядочить номенклатуру.
В 1920 г. Дж.Дреммонд скомбинировал термины Функа и Мак-Коллума. Для того, чтобы не привязывать витамины к определенной химической группе, он предложил опустить концевое "e", и с тех пор этот термин на языках, использующих латинский алфавит, пишется vitamin . Дреммонд также решил сохранить буквенное обозначение Мак-Коллума: в результате появились названия "витамин А" и "витамин В". Противоцинготный фактор получил имя "витамин С".
Спор о приоритете
Споры о приоритете возникли давно и, пожалуй, не утихли до сих пор. Кого же считать первооткрывателем витаминов? Наверное, так ставить вопрос нельзя. Многие ученые внесли свой вклад в это открытие. И все же наиболее весомым, по-видимому, можно считать вклад Н.И. Лунина, Х.Эйкмана, К.Функа и Ф.Г. Хопкинса.
В 1921 г. Хопкинс был удостоен медали Чендлера. В своей речи при вручении медали он признал себя пионером в открытии витаминов. И хотя Функ попытался оспорить приоритет Хопкинса, Нобелевской премии по физиологии и медицине за открытие витаминов в 1929 г. были удостоены только Хопкинс и Эйкман. Впрочем, в своей Нобелевской речи Хопкинс признал, что первые экспериментальные доказательства существования витаминов были получены Луниным.
А что же Лунин? Ему не пришлось продолжить исследовательскую работу. Он стал врачом-педиатром и в этом качестве приобрел известность и авторитет. Журнал "Педиатрия" в 1929 г. посвятил 50-летнему юбилею врачебной, общественной, научной и преподавательской деятельности Н.И. Лунина отдельный номер, целиком составленный из статей его учеников. Примечательно, что в среде педиатров было хорошо известно, какое выдающееся открытие сделал их коллега в начале своего творческого пути. Но советские витаминологи личностью Лунина не интересовались: организаторы 1-й Всесоюзной конференции по витаминам, проходившей в Ленинграде в 1934 г., не знали, что Лунин в то время жил и работал в том же городе, и не пригласили его принять участие в работе конференции.
В чем тут дело? В отсутствии интереса ко всему, что было до революции? Или в том, что Лунина не считали соотечественником? Среди витаминологов господствовало убеждение, что Лунин выполнил свою работу в Базеле, где впоследствии преподавал его руководитель Г.Бунге. Впрочем, Тарту в 20-30-е гг. тоже был "заграницей".
Зато в 40-е гг. все перевернулось. Утверждение приоритета российских ученых во всех областях науки стало государственной политикой. И тут сразу выяснилось, что Лунин сделал свое открытие не в заграничном Базеле, а в "отечественном" Тарту, и вообще, что его открытие замалчивалось. Появился десяток статей в защиту приоритета российской витаминологии. Некоторые авторы договаривались до того, что Функ и Хопкинс вообще не внесли ничего нового по сравнению с Луниным. Разумеется, все это издержки того времени. Все же, не умаляя роли других исследователей, важно отметить, что Лунин действительно внес выдающийся вклад в открытие витаминов.
Витаминов оказалось много
Но вернемся к истории исследования витаминов. В 20-е гг. с разработкой способов получения экспериментальных авитаминозов и совершенствованием методов очистки витаминов постепенно становилось ясно, что витаминов не два и не три, а гораздо больше.
Вначале выяснили, что "витамин А" на самом деле является смесью двух соединений, одно из которых предотвращает ксерофтальмию, а другое - рахит. За первым сохранилась буква А, а второе назвали "витамин D". Затем был открыт витамин Е, предотвращавший бесплодие у крыс, растущих на искусственной диете. Тогда же стало ясно, что и "витамин В" состоит как минимум из двух витаминов. Вот тут и начинается первая путаница: одни исследователи обозначили новый витамин, предотвращавший пеллагру у крыс и стимулировавший рост животных, буквой G, другие предпочли называть этот фактор "витамином В2 ", а фактор, предотвращавший бери-бери, - "витамином В1 ".
Термины "В1 " и "В2 " прижились. Фактор роста сохранил название "В2 ", а фактор, предотвращающий пеллагру крыс, стал "В6 ". Почему же использовали индекс 6? Разумеется, потому, что за это время появились "В3 ", "В4 " и "В5 ". Куда же они потом делись?
Название "В3 " получило в 1928 г. новое вещество, найденное в дрожжах и предотвращавшее дерматит у цыплят. Об этом веществе долгое время не было известно практически ничего, а десять лет спустя выяснилось, что оно идентично пантотеновой кислоте, которая изучалась как фактор роста дрожжей. В результате для этого витамина осталось название "пантотеновая ксилота".
В 1929 г. в дрожжах был обнаружен фактор, который поспешили назвать "витамином В4 ". Вскоре выяснилось, что этот фактор - не витамин, а смесь трех аминокислот (аргинина, глицина и цистина).
В 1930 г. появился термин "витамин В5 ": такое название было предложено для фактора, который впоследствии оказался смесью двух витаминов. Один из них - никотиновая кислота, которую изредка продолжают называть "витамин В5 ", другой - витамин В6 .
И в последующие годы продолжался тот же процесс: время от времени появлялись сообщения об открытиях новых факторов, и к букве "В" добавлялся новый индекс. Но повезло только индексу 12. Соединения с другими индексами либо оказались не витаминами или уже известными витаминами, либо их действие не получило подтверждения, либо название не получило широкого распространения.
А вскоре буквенная классификация витаминов утратила свое значение. В 30-е гг. за витамины по-настоящему взялись химики. И если в 1930 г. о химической природе витаминов практически ничего не было известно, то к 1940 г. этот вопрос был в основном решен.
Химики дали всем витаминам тривиальные химические названия. И эти названия постепенно стали вытеснять "буквы с цифрами": аскорбиновая кислота, токоферол, рибофлавин, никотиновая кислота и др. - эти термины стали общеупотребительными. Впрочем, многие биологи медики сохранили верность "буквам".
В 1976 г. Международный союз нутриционистов (от англ. nutrition - питание) рекомендовал сохранять буквенные обозначения в группе В только для витаминов В6 и В12 (по-видимому, из-за того, что эти витамины имеют несколько форм). Для остальных рекомендованы тривиальные названия веществ: тиамин, рибофлавин, пантотеновая кислота, биотин - или обобщающие термины: ниацин, фолацин .
Что такое пантенол
Пантенол является производным пантотеновой кислоты. В его молекуле кислотная группа заменена на спиртовую. В организме животных и человека пантенол легко превращается в пантотеновую кислоту, поэтому их витаминная активность сопоставима. Зато микроорганизмы не способны окислять пантенол, так что для микробов это вещество - яд.
Пантенол обладает важным достоинством: он очень хорошо всасывается при нанесении на кожу. Именно поэтому этот препарат так широко используется в дерматологии и косметике.
Но все-таки почему пантенол называют провитамином В5 ? Провитаминами принято называть природные вещества, которые в организме животных и человека превращаются в витамины. Так, b -каротин является провитамином А, эргостерин и 7-дегидрохолестерин - провитаминами D. Пантенол также способен превращаться в витамин - пантотеновую кислоту. Правда, в отличие от каротина и эргостерина пантенол - не природное вещество, а синтетический продукт.
А почему же "В5 "? Оказывается, среди множества названий, которых удостаивалась в 30-е гг. пантотеновая кислота, было и такое. И у этого названия остались приверженцы - еще в 70-е гг. оно встречалось в статьях французских медиков. Что ж, Франция, как известно, законодатель мод, в том числе и в области косметики.
СЛОВАРИК ТЕРМИНОВ
Витамин А - ретинол и его производные (ретиналь, ретиноевая кислота и др.), необходим для роста и дифференцировки тканей, процессов фоторецепции и репродукции, его недостаток вызывает ксерофтальмию.
Витамин С - аскорбиновая кислота, участвует в окислительно-восстановительных реакциях, его недостаток приводит к цинге .
Витамин D - группа родственных веществ, необходимых для роста костей (способствуют усвоению кальция и фосфора), его недостаток вызывает рахит .
Витамин Е - α-токоферол и родственные соединения, один из главных антиоксидантов в живых организмах, его недостаток вызывает бесплодие.
Витамин К - группа родственных веществ, участвующих в процессе свертывания крови.
Тиамин (витамин В1 ) - его производное, тиаминпирофосфат (кокарбоксилаза) входит в состав большого числа ферментов, участвующих в углеводном обмене, недостаток этого витамина приводит к заболеванию бери-бери .
Рибофлавин (витамин В2 ) - его производные входят в состав ферментов дыхательной цепи.
Пантотеновая кислота (витамин В3 ) - ее производные (кофермент А и др.) участвуют в важнейших процессах синтеза и распада веществ.
Витамин В6 - группа родственных веществ (пиридоксин, пиридоксаль, пиридоксамин), производные которых (пиридоксальфосфат и пиридоксаминфосфат) участвуют в обмене аминокислот.
Витамин В12 - группа родственных веществ (кобаламинов), входят в состав ферментов, участвующих во многих важных процессах синтеза и распада веществ, в том числе в процессе кроветворения.
Фолацин (витамин Вс ) - фолиевая кислота и родственные соединения, ее производное, тетрагидрофолиевая кислота, входит в состав ферментов, участвующих в важнейших синтетических процессах, в том числе в процессе кроветворения.
Ниацин (витамин РР) - никотиновая кислота и никотинамид, их производные, НАД и НАДФ, участвуют в огромном числе окислительно-восстановительных процессов.
Биотин (витамин Н) - входит в состав ферментов, осуществляющих карбоксилирование (присоединение молекулы углекислого газа) органических кислот.
АВИТАМИНОЗЫ
Бери-бери - заболевание, связанное с недостатком витамина В1 . Характеризуется распространенным поражением периферических нервов конечностей. Болезнь получила широкое распространение в странах Восточной и Юго-Восточной Азии в XIX в., когда главный пищевой продукт этих стран, рис, стали очищать от оболочки ("полированный" рис).
Ксерофтальмия - поражение глаз, выражающееся в сухости конъюнктивы и роговицы. Одна из главных причин заболевания - недостаток витамина А.
Пеллагра - заболевание, связанное с недостатком ниацина. Проявляется в поражении кожи, пищеварительного тракта и нервной системы. Распространена в странах, где основной продукт питания - кукуруза.
Рахит - заболевание детей, связанное с недостатком витамина D. Характеризуется размягчением костей.
Цинга - Заболевание, связанное с недостатком витамина С. Возникает обычно при отсутствии в рационе свежих овощей и фруктов. Часто наблюдалась у участников северных и морских экспедиций. Характеризуется кровоточивостью десен, выпадением зубов и т.п.
Аденозинтрифосфат тиамин
Аденозинтрифосфат тиамин (AТФТ) или тиаминилированный аденозинтрифосфат, недавно был обнаружен в кишечной палочке, где он накапливается в результате углеродного голодания. В E.coli, AТФТ может составлять до 20% от общего тиамина. Кроме того, в меньшем количестве он присутствует в дрожжах, корнях высших растений и тканях животных.
Аденозин тиамин дифосфат
Аденозин тиамин дифосфат (АТДФ) или тиаминилированный АДФ, существует в небольших количествах в печени позвоночных, однако его роль все еще остается неизвестной.
Дефицит тиамина
Производные тиамина и тиамин-зависимые ферменты присутствуют во всех клетках организма, и таким образом, дефицит оказывает влияние на все системы органов. Нервная система оказывается особенно чувствительной к дефициту тиамина, из-за ее зависимости от окислительного метаболизма. Дефицит тиамина обычно проявляется подостро и может привести к метаболической коме и смерти. Недостаток тиамина может быть вызван недоеданием, диетой с высоким содержанием продуктов, богатых тиаминазой (сырая пресноводная рыба, сырые моллюски, папоротники) и / или продуктов с высоким содержанием анти-тиаминных факторов (чай, кофе, орех катеху), грубыми нарушениями питания, связанными с хроническими заболеваниями, такими как алкоголизм, желудочно-кишечные расстройства, ВИЧ, СПИД и частая рвота. Предполагается, что множество людей, страдающих диабетом, страдают от дефицита тиамина, что может быть связано с некоторыми возможными осложнениями. Синдромы, вызванные дефицитом тиамина, включают в себя: бери-бери, синдром Вернике-Корсакова и оптическую нейропатию. Тиамин также может быть использован для лечения потери памяти при болезни Альцгеймера и алкогольной болезни мозга.
Болезнь Альцгеймера
Дефицит тиамина может оказывать пагубное воздействие на холинергическую систему. При болезни Альцгеймера тиамин-зависимые ферменты могут быть изменены; следовательно, тиамин в фармакологических дозах (от 3 до 8 г/сут перорально) может оказывать мягкое благотворное влияние при деменции типа Альцгеймера. Фурсультиамин (ТТФД), производное тиамина, оказывает умеренный положительный эффект на пациентов с болезнью Альцгеймера, в качестве альтернативного лечения больших доз тиамин гидрохлорида. Все еще не ясны механизм и этиология воздействия тиамина на болезнь Альцгеймера, а также пока что полностью не подтверждены доказательства его эффективности.
Бери-бери
Бери-бери является неврологическим и сердечно-сосудистым заболеванием. Три основные формы заболевания – сухое бери-бери, влажное бери-бери и младенческое бери-бери.
Сухое бери-бери характеризуется главным образом периферической нейропатией, то есть симметричным ухудшением сенсорных, моторных и рефлекторных функций, более влияющим на дистальные, нежели проксимальные, сегменты конечностей и вызывающим болезненность икроножных мышц.
Тем не менее, недавно было признано, что периферическая нейропатия (покалывание или онемение в конечностях), связанная с дефицитом тиамина, может также быть представлена аксональной нейропатией (частичным параличом или потерей чувствительности). Периферическая нейропатия может проявляться подострой двигательной аксональной нейропатией, имитирующей синдром Гийена-Барре; или как подострая сенсорная атаксия.
Влажное бери-бери связано со спутанностью сознания, мышечной атрофией, отеками, тахикардией, кардиомегалией и застойной сердечной недостаточностью в дополнение к периферической невропатии.
Младенческое бери-бери встречается у детей, кормящихся грудью, если у матери имеется дефицит тиамина (который внешне может никак не проявляться). Расстройство у младенцев может выражаться в сердечных, афонических или псевдоминингитных формах. Младенцы с сердечным бери-бери часто громко и пронзительно плачут, также наблюдается рвота и тахикардия. Не редки при этом судороги, и если быстро не ввести в организм ребенка тиамин, может наступить смерть.
После введения тиамина улучшение наблюдается, как правило, в течение 24 часов. Улучшения периферической нейропатии может потребовать нескольких месяцев лечения с помощью тиамина.
Алкогольная болезнь мозга
Нервные и другие поддерживающие клетки (например, клетки глии) нервной системы требуют наличия тиамина. Примеры неврологических расстройств, связанных со злоупотреблением алкоголем, включают энцефалопатию Вернике (ЭВ, синдром Вернике-Корсакова) и психоз Корсакова (алкогольный амнестический синдром), а также когнитивные нарушения различной степени. Энцефалопатия Вернике является наиболее часто встречающимся проявлением дефицита тиамина в западном обществе, хотя она также может наблюдаться у больных с нарушениями питания и вследствие других причин, таких как желудочно-кишечные заболевания, инфекции ВИЧ-СПИД, избыточное применение парентеральной глюкозы или переедание без адекватного количества B-витаминных добавок. Это поразительное нервно-психическое расстройство характеризуется параличом движений глаз, нарушением стояния и ходьбы и заметным ухудшением психических функций.
Оптическая нейропатия
При дефиците тиамина также может наблюдаться оптическая нейропатия, характеризующаяся двусторонней потерей зрения, центроцекальной скотомой и нарушениями цветового восприятия. Офтальмологический анализ обычно показывает двусторонний отек диска зрительного нерва в острой фазе и двустороннюю атрофию зрительного нерва.
Алкоголики испытывают дефицит тиамина по следующим причинам:
Недостаточное потребление питательных веществ: алкоголики, как правило, потребляют тиамин в количествах, меньше рекомендованных.
Снижение поглощения тиамина из желудочно-кишечного тракта: Активный транспорт тиамина в энтероциты искажается при остром воздействии алкоголя.
Запасы тиамина в печени снижаются из-за стеатоза или фиброза печени.
Нарушение использование тиамина: из-за хронического потребления алкоголя уровень , необходимого для связывания тиамина с ферментами, использующими тиамин в клетке, также является недостаточным. Неэффективное использование тиамина, который достигает клетку, еще больше усугубляет дефицит.
Этанол сам по себе ингибирует транспорт тиамина в желудочно-кишечном тракте и блокирует фосфорилирование тиамина в виде его кофактора (ТДФ).
Считается, что синдром Корсакова (ухудшение функций мозга), наблюдается у пациентов, изначально диагнозированных ЭВ. Это амнестически-конфабуляторный синдром, характеризующийся ретроградной и антероградной амнезией, нарушением концептуальных функций и снижением спонтанности и инициативности.
При улучшении питания и прекращении потребления алкоголя устраняются и некоторые нарушения, связанные с дефицитом тиамина, в частности, плохое функционирование мозга, однако в более тяжелых случаях, синдром Вернике-Корсакова оставляет необратимые повреждения.
Дефицит тиамина у домашней птицы
Поскольку большинство используемой в птичьих кормах пищи содержит достаточное количество витаминов для удовлетворения их потребностей, при такой «коммерческой» диете у птиц не наблюдается авитаминоза. Так, по крайней мере, считалось в 1960-х годах. Пожилые куры показывают признаки авитаминоза через 3 недели после начала дефицитной диеты. У молодых птенцов эти признаки могут начать проявляться уже в 2-недельном возрасте. У молодых птенцов заболевание начинается внезапно. Наблюдается анорексии и нетвердая походка. Позже проявляются опорно-двигательные нарушения, начиная с видимого паралича сгибателей пальцев. Характерная позиция называется «созерцание звезд», когда тело цыпленка «держится на скакательных суставах и голове в опистотонусе». Ответ организма на введение витамина довольно быстр, улучшение возникает уже через несколько часов. Дифференциальная диагностика включает дефицит рибофлавина и птичий энцефаломиелит. При дефиците рибофлавина характерным симптомом являются «подвернутые пальцы». Мышечный тремор является типичным для инфекционного энцефаломиелита. Терапевтический диагноз может быть поставлен только после лечения пострадавших птиц тиамином. Если в течение нескольких часов отклика не наблюдается, дефицит тиамина можно исключить.
Дефицит тиамина у жвачных животных
Полиоэнцефаломаляция (ПЭМ) – наиболее распространенное расстройство дефицита тиамина у молодых жвачных и нежвачных животных. Симптомы ПЭМ включают обильную, но переходную, диарею, вялость, круговые движения, «созерцание звезд» или опистотонус (конвульсивное вытягивание головы за шею) и тремор мышц. Наиболее распространенной причиной является кормление животных пищей с высоким содержанием углеводов, что приводит к разрастанию бактерий-продуцентов тиаминазы, также возможен диетический прием тиаминазы (например, из папоротника) или ингибирование поглощения тиамина при высоком потреблении серы. Еще одной причиной ПЭМ является инфекция Clostridium Sporogenes, или Bacillus aneurinolyticus. Эти бактерии вырабатывают тиаминазы, которые вызывают острый дефицит тиамина у пострадавших животных.
Идиопатическое паралитическое заболевание у диких птиц, рыб и млекопитающих
В последнее время дефицит тиамина определялся в качестве причины паралитического заболевания, поражающего диких птиц в районе Балтийского моря, начиная с 1982 года. При этой болезни птицы испытывают трудности в поддержании крыльев в сложенном вдоль тела положении во время отдыха, теряют способность к полету и голос, также возможен паралич крыльев и ног и смерть. Заболевание сказывается в первую очередь на птицах весом 0,5-1 кг, таких как серебристая чайка (Larus argentatus), Обыкновенный скворец (Sturnus vulgaris) и обыкновенная гага (Somateria mollissima). Исследователи отмечают: «вследствие того, что исследуемые виды занимают широкий спектр экологических ниш и позиций в пищевой сети, мы не отрицаем возможности того, что другие классы животных также могут страдать от дефицита тиамина». В графствах Блекинг и Скон (юг Швеции) с начала 2000-х началась массовая гибель птиц, особенно серебристой чайки. Совсем недавно были затронуты виды и других классов. За последние годы в знаменитой реке Mörrumsån возросла смертность лосося (Salmo salar). Млекопитающее Евразийский Лось (Alces аlces) также страдает в необычайно крупных количествах. В ходе анализа выяснилось, что общей причиной этих бедствий является недостаток тиамина. В апреле 2012 года Окружной административный совет Блекинга посчитал сложившуюся ситуацию настольно тревожной, что выступил с просьбой к правительству Швеции о проведении более тщательного исследования.
Анализ и диагностическое тестирование
Положительный результат диагностики дефицита тиамина может быть установлен путем измерения активности фермента транскетолазы в эритроцитах (количественный анализ активации транскетолазы эритроцитов). Тиамин и его фосфатные производные также могут быть обнаружены непосредственно в кровотоке, тканях, пищевых продуктах, кормах для животных и фармацевтических препаратах, после преобразования тиамина в его флуоресцентное производное тиохром (тиохромный анализ) и разделение при помощи высокоэффективной жидкостной хроматографии (ВЭЖХ). В последние годы возникает все большее количество методов капиллярного электрофореза и методов капиллярных ферментативных реакций в качестве потенциальных альтернативных методов определения и мониторинга тиамина в образцах. Нормальная концентрация тиамина в ЭДТА-крови (кровь с этилендиаминтетрауксусной кислотой) составляет около 20-100 мкг/л.
Генетические заболевания
Генетические заболевания, связанные с нарушением транспорта тиамина, редки, но достаточно серьезны. Тиаминзависимая мегалобластная анемия (ТЗМА) с сахарным диабетом и нейросенсорной тугоухостью – это аутосомно-рецессивные расстройства, вызванные мутациями в гене SLC19A2, транспортера тиамина с высоким сродством. Пациенты, страдающие ТЗМА, не проявляют признаков системного дефицита тиамина, так как в транспортной системе тиамина предполагается избыточность. Это привело к открытию второго транспортера тиамина с высоким сродством, SLC19A3. Болезнь Ли (подострая некротизирующая энцефаломиелопатия) – наследственное заболевание, которое затрагивает главным образом детей в первые годы жизни и является неизменно фатальным. Патологические сходство между болезнью Ли и ЭВ ведет к предположению, что их причиной является какой-либо дефект в метаболизме тиамина. Наиболее последовательными были сведения об аномалии в активации пируватдегидрогеназного комплекса. Другие нарушения, в которые включались предполагаемые роли тиамина – это подострая некротизирующая энцефаломиелопатия, паранеопластический синдром и Нигерийская сезонная атаксия. Кроме того, сообщалось о нескольких наследственных нарушениях ТДФ-зависимых ферментов, которые могут реагировать на лечение тиамином.
История
Тиамин был первым описанным водорастворимым витамином. Его открытие породило ряд других открытий и к возникновению самого понятия «витамины». В 1884 году Канехиро Такаки (1849-1920), главный хирург японского флота, отклонил господствующую тогда микробную теорию авитаминоза и предположил, что это заболевание может быть связано с недостатками в рационе. Улучшив рацион моряков на военном корабле, он обнаружил, что замена белого риса (который составлял основу их рациона) ячменем, мясом, молоком, хлебом, овощами, вызвала практически полную ликвидацию авитаминоза во время 9-месячного морского путешествия. Тем не менее, так как Такаки добавил в их рацион большое множество разнообразных продуктов питания, был сделан неверный вывод о пользе увеличения потребления азота, так как в то время витамины были неизвестными веществами. Кроме того, представителей ВМФ не удалось убедить в необходимости столь дорогой программы диетического улучшения, тем более многие мужчины продолжали умирать от авитаминоза даже во время русско-японской войны 1904-5. Однако в 1905 году, после того, как в рисовых отрубях был обнаружен антиавитаминозный фактор (удаляемый из белого риса при обработке) и в коричневом ячменном рисе, Такаки был вознагражден титулом барона, после чего он получил прозвище «Ячменный барон». В 1897 году Христиан Эйкман (1858-1930), военный врач в Голландской Ост-Индии, обнаружил, что у птиц, питающихся вареным шлифованным рисом, начинает развиваться паралич, который можно вылечить, прекратив кормить птиц шлифованным рисом. Он утверждал, что бери-бери развивается из-за нервного «яда» в эндосперме риса, а внешние слои зерна дают организму защиту. Его помощник, Геррит Гриджинс (1865-1944), в 1901 году правильно интерпретировал связь между чрезмерным потреблением шлифованного риса и авитаминозом. Он заключил, что во внешних слоях рисового зерна содержатся необходимые организму питательные вещества, которые удаляются при шлифовке. В 1929 году Эйкману, в конечном счете, была присуждена Нобелевская премия по физиологии и медицине, потому что его наблюдения привели к открытию витаминов. Имя этим соединениям дал Казимир Функ. В 1911 году Казимир Функ выделил из рисовых отрубей антинейритические вещества, которое он назвал «витамины» (полагая, что они содержат аминогруппу). В 1926 году голландские химики, Баренд Конрад Петрус Янсен (1884-1962) и его ближайший сотрудник Фредерик Виллем Донат (1889-1957), смогли изолировать и кристаллизовать активное вещество, структура которого была определена в 1934 году Руннелсом Робертом Уильямсом (1886 -1965), химиком из США. Эта же группа в 1936 году синтезировала тиамин («серосодержащий витамин»). Тиамин изначально назвали «аневрин» (витамин для борьбы с нейритом). Сэр Рудольф Петерс из Оксфорда представил голубей, диета которых была лишена тиамина, в качестве модели для понимания того, как дефицит тиамина может привести к возникновению патологически-физиологических симптомов бери-бери. Действительно, кормление голубей шлифованным рисом приводит к легко узнаваемому сокращению мышц шеи и головы, называемому опистотонус. В отсутствии лечения животное умирало через несколько дней. Введение тиамина на стадии опистотонуса ведет к полному излечению животных в течение 30 мин. Поскольку в мозге голубей не наблюдалось никаких морфологических изменений до и после лечения тиамином, Питерс ввел понятие «биохимическое поражение». Когда Лохман и Шустер (1937) показали, что дифосфорилированное производное тиамина (тиамин дифосфат, ТДФ) является кофактором, необходимым для окислительного декарбоксилирования пирувата (реакция, известная сейчас как катализируемая пируватом дегидрогеназа), казалось, был выяснен механизм действия тиамина в клеточном метаболизме. В настоящее время эта точка зрения кажется упрощенной: пируват-дегидрогеназа является лишь одним из нескольких ферментов, требуемых тиамин дифосфату в качестве кофактора, кроме того, с тех пор были обнаружены другие производные тиамин фосфата, которые также могут влиять на симптомы, наблюдаемые при дефиците тиамина. Наконец, механизм, посредством которого тиамин фрагмент ТДФ проявляет свою функцию кофермента при протонном замещении в положении 2 на тиазольном кольце, был открыт Рональдом Бреслоу в 1958 году.
Исследования
Исследования в этой области в основном касаются механизмов, посредством которых дефицит тиамина приводит к гибели нейронов по отношению к психозу Вернике-Корсакова. Другая важная тема фокусируется на понимании молекулярных механизмов, участвующих в катализе ТДФ. Исследование было посвящено пониманию возможных не-кофакторных ролей других производных, таких как ТТФ и AТТФ.
Дефицит тиамина и селективная гибель нейронов
Экспериментально вызванная бери-бери полинейропатия у кур может быть хорошим примером для изучения этой формы нейропатии с учетом диагностики и лечения. В ходе исследований с использованием крыс была обнаружена связь между дефицитом тиамина и канцерогенезом толстой кишки. Крысы также были использованы в исследовании энцефалопатии Вернике. Крысы, лишенные тиамина, являются классической моделью системного окислительного стресса, использующиеся в исследованиях болезни Альцгеймера.
Каталитические механизмы тиамин дифосфат-зависимых ферментов
Множество работ посвящено пониманию взаимосвязи между ТДФ и ТДФ-зависимых ферментов в катализе.
Не-кофакторные роли производных тиамина
В большинстве клеток множества организмов, включая бактерий, грибы, растения и животных, существуют тиаминовые соединения, отличные от ТДФ. Среди этих соединений – тиамин трифосфат (ТТФ) и аденозин тиамин трифосфат (AТТФ), которые обладают не-кофакторными ролями, хотя в настоящее время точно не известно, в какой именно степени они влияют на симптомы заболевания.
Новые производные тиамина
До сих пор продолжают обнаруживаться новые производные тиамина фосфата, что подчеркивает сложность метаболизма тиамина. Производные тиамина с улучшенной фармакокинетикой могут оказаться эффективными в облегчении симптомов дефицита тиамина и других заболеваний, связанных с тиамином, таких, как нарушение метаболизма глюкозы при диабете. Эти соединения, среди прочих, включают в себя аллитиамин, просультиамин, фурсультиамин, бенфотиамин и .
Стойкие карбены
Производство фуроина из фурфурола катализируется тиамином через относительно стабильный карбен (органическую молекулу, содержащую несвязанные валентные пары электронов на углеродном центре). Эта реакция, изучаемая в 1957 году Р. Бреслоу, была первым доказательством существования стойких карбенов.


 Активная форма:
кофермент тиаминдифосфат (ТДФ).
Активная форма:
кофермент тиаминдифосфат (ТДФ).
 Активные формы
: коферменты флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД).
Активные формы
: коферменты флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД).
 Активная форма:
кофермент пиридоксальфосфат.
Активная форма:
кофермент пиридоксальфосфат.
 Активная форма:
коферменты никотинамидадениндинуклеотид (НАД) и никотинамидадениндинук-леотидфосфат (НАДФ).
Активная форма:
коферменты никотинамидадениндинуклеотид (НАД) и никотинамидадениндинук-леотидфосфат (НАДФ).
 Активная форма:
кофермент тетрагидрофолиевая кислота.
Активная форма:
кофермент тетрагидрофолиевая кислота.